巧用活塞分離干燥混合氣 CO?與CO分離實驗設計與試劑選擇
分離和干燥一氧化碳(CO)與二氧化碳(CO?)的混合氣體,需要利用兩者化學性質的顯著差異。二氧化碳是酸性氧化物,能與堿液反應;而一氧化碳在常溫下化學性質穩定,不與堿反應。因此,實驗的核心是利用這一特性進行分離,再分別進行干燥以獲得純凈氣體。
一、 實驗裝置與操作流程概述
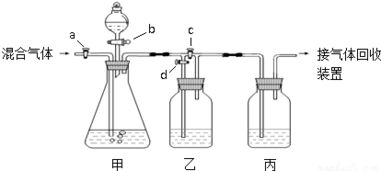
裝置如圖所示,包含四個可獨立控制的活塞a、b、c、d,連接著氣體通路和試劑儲瓶。實驗前所有活塞關閉。基本流程為:混合氣體通入→吸收CO?(分離)→分別干燥CO和富集CO?的溶液→最終收集純凈、干燥的CO和CO?氣體。
二、 關鍵試劑選擇與作用
- 吸收劑(用于分離CO?):
- 首選試劑:濃氫氧化鈉(NaOH)溶液。
* 作用原理:CO?與NaOH反應生成碳酸鈉(Na?CO?)或碳酸氫鈉(NaHCO?),從而被液體完全吸收。化學方程式為:
> 2NaOH + CO? → Na?CO? + H?O (CO?量適中)
> NaOH + CO? → NaHCO? (CO?過量)
- 優點:吸收效率極高,反應迅速、徹底,是實驗室最常用的CO?吸收劑。
- 替代選擇:澄清石灰水[Ca(OH)?溶液]。但其濃度低,吸收容量有限,且生成的碳酸鈣(CaCO?)微溶可能堵塞管路,故非最優選。
- 干燥劑(用于氣體干燥):
- 對于分離出的CO氣體:
- 首選試劑:濃硫酸(H?SO?) 或 無水氯化鈣(CaCl?)。
- 原理:二者均為中性或酸性干燥劑,具有強烈的吸水性,且不與CO發生任何反應。
- 對于從吸收液中釋放出的CO?氣體:
- 釋放CO?:需向吸收了CO?的NaOH溶液中加入強酸(如稀鹽酸HCl或稀硫酸H?SO?),使碳酸鹽分解釋放出CO?氣體。
- 干燥CO?:釋放出的CO?含有水蒸氣,應使用濃硫酸(H?SO?)進行干燥。
- 注意:不能用堿性干燥劑(如堿石灰)干燥CO?,因其會發生反應。
三、 實驗步驟簡述(配合活塞操作)
- 混合氣體通入與CO?吸收:打開活塞a和b,讓混合氣體緩慢通入盛有濃NaOH溶液的洗氣瓶(或反應瓶)。CO?被吸收,不含CO?的CO氣體(混有水蒸氣)從出口導出。關閉a、b。
- CO的干燥與收集:將上述導出的濕潤CO氣體,通過打開活塞c,通入盛有濃硫酸的干燥瓶進行干燥,隨后即可收集到純凈干燥的CO氣體。操作完畢后關閉c。
- CO?的釋放與干燥:
- 關閉氣體通路,打開活塞d,向已吸收CO?的NaOH溶液中緩慢加入稀鹽酸。此時會產生純凈的CO?氣體,但含有水蒸氣及可能揮發出的少量HCl。
- 將此氣體先通過一個盛有少量水或飽和NaHCO?溶液的洗氣瓶(圖中可增設,或利用另一通路)以除去HCl,再通入濃硫酸干燥瓶中進行干燥。
- 最后收集純凈、干燥的CO?氣體。
四、
成功完成此實驗的關鍵在于:
- 分離試劑:選擇濃氫氧化鈉溶液高效吸收CO?。
- 干燥試劑:對兩種氣體均優先選用濃硫酸作為干燥劑。
- 釋放試劑:使用稀鹽酸從吸收液中重新獲得CO?。
- 活塞控制:通過精準控制活塞a、b、c、d的順序開閉,實現氣體的定向流動、試劑的分步加入,從而避免氣體交叉污染,確保分離和干燥的徹底性。
此裝置設計體現了在“液體分離及純凈設備制造”中,通過模塊化閥門控制、針對不同物質性質選擇特異性試劑,從而實現復雜混合物高效分離與提純的核心思想。
如若轉載,請注明出處:http://m.yuyuez.cn/product/26.html
更新時間:2026-05-09 15:06:42